NOGGO S15 - فراستروك
دراسة للمرضى الذين يعانون من سرطان المبيض المتكرر أو المنتكس.
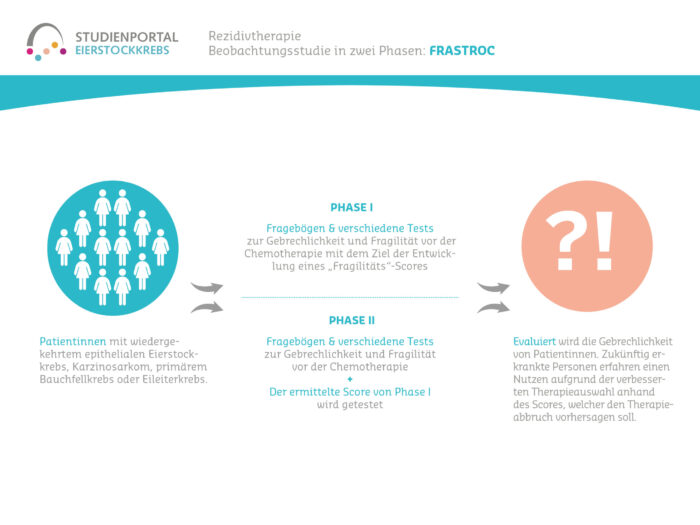
دراسة لمرضى سرطان المبيض المتكرر أو المنتكس
إن دراسة FraStROC هي دراسة غير تداخلية واستشرافية ومتعددة المراكز تقوم على الملاحظة يتم فيها تقييم ضعف وهشاشة مرضى سرطان المبيض في حالة تكرار الإصابة أثناء العلاج الكيميائي. تُجرى الدراسة على مرحلتين.
ما هو الهدف من الدراسة؟
تهدف الدراسة إلى تقييم العلامات الالتهابية والخلل الوظيفي للأعضاء والاختبارات الوظيفية ومقاييس تقييم الشيخوخة والنتائج التي أبلغ عنها المريض من حيث قدرتها على التنبؤ بالسمية الدموية أو السمية غير الدموية.
كيف يتم تنظيم الدراسة؟
هذه دراسة استشرافية متعددة المراكز وغير تداخلية وقائمة على الملاحظة على مرحلتين للمرضى الذين يعانون من سرطان المبيض الظهاري أو سرطان المبيض السرطاني أو سرطان قناة فالوب أو سرطان الصفاق الأولي الذين يحتاجون إلى علاج أحادي للمرض المتكرر وشاركوا في علاج نظامي واحد سابق على الأقل.
الخطوتان 1 و 2:
في الدراسة، يتم تقييم الجوانب الديموغرافية والسريرية والمرضية للمرضى، وتوثيق التدابير المتخذة قبل بدء العلاج الكيميائي وتقييم السمية لمدة عام واحد من بداية العلاج (المتابعة).
في الخطوة الأولى من الدراسة، سيتم تحديد درجة الضعف على أساس البيانات التي تم جمعها من أجل تقدير احتمال وقف العلاج الكيميائي بسبب الآثار الجانبية. في الخطوة الثانية من الدراسة، سيتم اختبار الدرجة التي تم تحديدها (التحقق من صحتها).
هل هناك أي مخاطر؟
لا، إنها دراسة قائمة على الملاحظة.
متطلبات المشاركة
هل يمكنني المشاركة في هذه الدراسة؟
أهم معايير الإدراج والاستبعاد:
يجب على المرضى تقديم إقرار خطي بالموافقة مسبقاً وأن يكون عمرهم 18 عاماً على الأقل:
- لديك تشخيص مؤكد من الناحية النسيجية لسرطان المبيض الظهاري أو سرطان المبيض السرطاني أو سرطان الصفاق الأولي أو سرطان قناة فالوب
- مصابًا بسرطان متكرر
- مؤهلون للعلاج الكيميائي الأحادي باستخدام باكليتاكسيل أو دوكسوروبيسين أو توبوتيكان أو تريوسولفان مع استخدام اختياري للبيفاسيزوماب
- تلقوا نظامًا علاجيًا سابقًا واحدًا على الأقل لسرطان المبيض (مسموح به من الخط الثاني من العلاج)
- لها عمر متوقع لا يقل عن 12 أسبوعًا.
المرضى غير المؤهلين:
يتم استبعاد المرضى إذا:
- يكونون مؤهلين فقط للعلاج الكيميائي المركب أو علاج المداومة بعد التخطيط للعلاج الكيميائي أو العلاج الإشعاعي السابق.
بالإضافة إلى ذلك، هناك معايير أخرى يجب استيفاؤها. يجب على المرضى المهتمين التحدث إلى أحد الباحثين في مركز الدراسة الذي يمكنه التحقق مما إذا كانوا مؤهلين لهذه الدراسة.
هل أنت مهتم بالدراسة؟
يُرجى التواصل مع فريقك الطبي (طبيب أمراض النساء أو طبيب الأورام) مع ملف PDF هذا. سيقومون بالتحقق مما إذا كانت الدراسة مناسبة لكِ أم لا وإحالتك إلى مركز الدراسة.


