NOGGO S15 – FraStROC
Studie für Patientinnen mit wiederkehrendem oder wiedergekehrtem Eierstockkrebs.
STUDIE FÜR PATIENTINNEN MIT WIEDERKEHRENDEM ODER WIEDERGEKEHRTEM EIERSTOCKKREBS
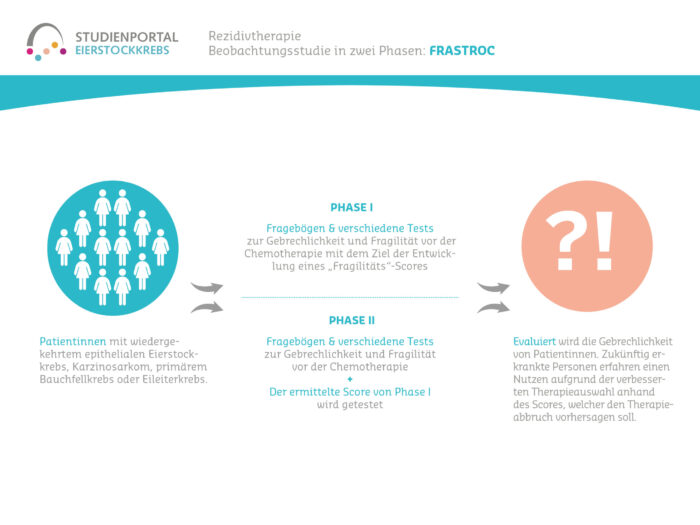
Die FraStROC-Studie ist eine nicht-interventionelle, prospektive, multizentrische Beobachtungsstudie, in der die Gebrechlichkeit und Fragilität von Ovarialkarzinom-Patientinnen in der Rezidivsituation während der Chemotherapie evaluiert wird. Die Studie erfolgt in zwei Phasen.
Was ist das Ziel der Studie?
Das Ziel der Studie ist die prospektive Bewertung von Entzündungsmarkern, Organfunktionsstörungen, Funktionstests und Maßnahmen zur geriatrischen Beurteilung sowie des von Patientinnen berichteten Ergebnisses hinsichtlich ihrer Fähigkeit, die hämatologische Toxizität oder nicht-hämatologische Toxizität vorherzusagen.
Wie ist der Ablauf der Studie?
Dies ist eine prospektive, multizentrische, nicht-interventionelle Beobachtungsstudie in 2 Stufen für Patientinnen mit epithelialem Eierstockkrebs oder Karzinosarkom (EOC), Eileiterkrebs (FTC) oder primärem Bauchfellkrebs (PPC), die wegen wiederkehrender Krankheit eine Monotherapie benötigen und an mindestens einer vorherigen systemischen Behandlung teilgenommen haben.
Schritt 1 und 2:
In der Studie werden demografische, klinische und pathologische Aspekte der Patientinnen bewertet, sowie die Maßnahmen vor Beginn der Chemotherapie dokumentiert und eine Beurteilung der Toxizität für ein Jahr ab Behandlungsstart vorgenommen (Follow-up).
Im ersten Schritt der Studie soll anhand der erhobenen Daten eine Gebrechlichkeitsbewertung (Fragilitäts-Score) ermittelt werden, um abschätzen zu können, wie hoch die Wahrscheinlichkeit ist, dass die Chemotherapie aufgrund von Nebenwirkungen abgebrochen werden muss. Im zweiten Schritt der Studie wird der ermittelte Score getestet (validiert).
Gibt es Risiken?
Nein, es ist eine Beobachtungsstudie.
TEILNAHMEVORAUSSETZUNGEN
Kann ich an dieser Studie teilnehmen?
Wichtigste Ein- und Ausschlusskriterien:
Patientinnen müssen vorab eine schriftliche Einverständniserklärung vorlegen, mindestens 18 Jahre alt sein sowie:
- eine histologisch bestätigte Diagnose eines epithelialen Eierstockkrebses, Karzinosarkoms, primären Bauchfellkrebses oder Eileiterkrebses haben
- eine wiederkehrende Krebserkrankung haben
- für eine Monochemotherapie mit Paclitaxel, Doxorubicin (PLD), Topotecan oder Treosulfan mit optionaler Anwendung von Bevacizumab in Frage kommen
- mindestens ein vorheriges Behandlungsschema für Eierstockkrebs erhalten haben (ab der zweiten Behandlungslinie zulässig)
- eine Lebenserwartung von mindestens 12 Wochen haben.
Nicht in Frage kommende Patientinnen:
Patientinnen werden ausgeschlossen, wenn:
- sie nur für eine Kombinationschemotherapie oder Erhaltungstherapie nach vorheriger Chemotherapie in Frage kommen oder eine Strahlentherapie geplant ist.
Darüber hinaus gibt es weitere Kriterien, die erfüllt sein müssen. Interessierte Patientinnen sollten mit einem Prüfarzt/-ärztin an einem Studienzentrum sprechen, der/die prüfen kann, ob sie für diese Studie in Frage kommen.
SIE INTERESSIEREN SICH FÜR DIE STUDIE?
Wenden Sie sich gerne mit diesem PDF an Ihr betreuendes Ärzteteam (Gynäkologen oder Onkologen). Diese werden prüfen, ob die Studie für Sie in Frage kommt und Sie zu einem Studienzentrum vermitteln.


