ENGOT-OV34 Studie mit enttäuschenden Ergebnissen bei rezidiviertem Eierstockkrebs
Eine kürzlich durchgeführte Studie (AGO-OVAR 2.29/ENGOT-ov34), die auf der ASCO 2024 präsentiert wurde, einem der wichtigsten Krebskongresse der Welt, untersuchte die Kombination von Atezolizumab mit einer nicht-platinbasierten Chemotherapie und Bevacizumab bei Patientinnen mit rezidiviertem Eierstockkrebs. Die Ergebnisse zeigten, dass diese Kombination die Gesamtüberlebenszeit (OS) und das progressionsfreie Überleben (PFS) im Vergleich zu Placebo nicht signifikant verbesserte.
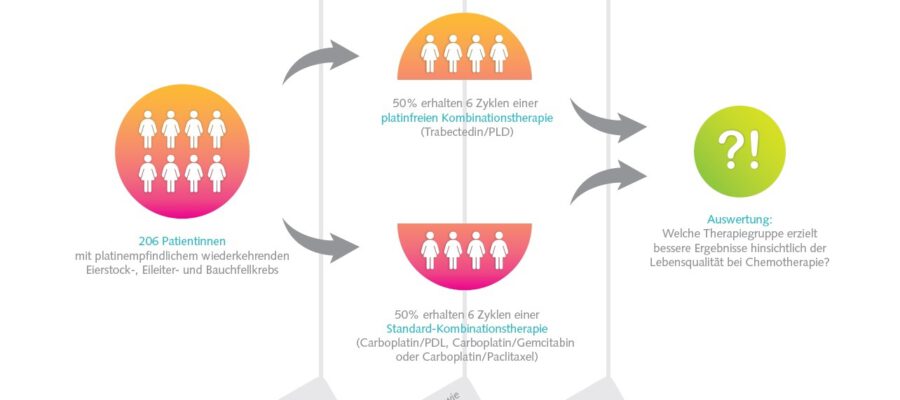
In der Studie wurden 574 Patientinnen zufällig entweder Atezolizumab oder einem Placebo zugeteilt, zusätzlich zu Bevacizumab und entweder wöchentlichem Paclitaxel oder pegylierter liposomaler Doxorubicin. Die Ergebnisse zeigten, dass das mediane progressionsfreie Überleben in der Atezolizumab-Gruppe 6,4 Monate betrug, verglichen mit 6,7 Monaten in der Placebo-Gruppe, was keinen statistisch signifikanten Unterschied darstellte. Auch das mediane Gesamtüberleben unterschied sich nicht signifikant zwischen den beiden Gruppen (14,2 Monate für Atezolizumab vs. 13,0 Monate für Placebo).
Zusammenfassend lässt sich sagen, dass die Zugabe von Atezolizumab zu einer nicht-platinbasierten Chemotherapie und Bevacizumab bei rezidiviertem Eierstockkrebs keine signifikante Verbesserung des Überlebens brachte. Diese Ergebnisse unterstreichen die Notwendigkeit weiterer Forschung, um wirksamere Behandlungsstrategien für diese Patientengruppe zu finden.
https://engot.esgo.org/clinical-trials/current-clinical-trials/ovarian/
Quelle: https://ascopubs.org/doi/10.1200/JCO.2024.42.17_suppl.LBA5501